Trong quy trình hướng dẫn của CDC Hoa kỳ (FDA cấp EUA) đã loại bỏ việc phát hiện gene N3 sau thời gian đầu thực hiện xét nghiệm Covid-19, thì không hiểu sao vừa qua bộ kit xét nghiệm Covid-19 của 1 đơn vị sản xuất trong nước có chứa thành phần phát hiện gene N3 lại trúng gói thầu mua sắm kit real-time RT-PCR phát hiện SARS-CoV-2 do Bộ Y tế giao cho Bệnh viện Nhi Trung ương thực hiện?
Khi đại dịch Covid-19 xảy ra, 2 cơ quan về y tế hàng đầu thế giới là Tổ chức Y tế thế giới (WHO) và Trung tâm Kiểm soát Dịch bệnh Hoa Kỳ (CDC) luôn là đơn vị đầu tiên đưa ra các hướng dẫn, quy trình liên quan đến việc phòng chống dịch, trong đó đặc biệt quan trọng là quy trình xét nghiệm và được cả thế giới sẽ tham khảo và áp dụng. Trong đó có cả Bộ Y tế Việt Nam, luôn có sự hướng dẫn áp dụng rất chặt chẽ quy trình của 2 tổ chức này. Xét nghiệm phát hiện 1 tác nhân, đặc biệt là các tác nhân rất mới mẻ như SARS-CoV-2 luôn được cải tiến qua thời gian để đơn giản, hiệu quả và đặc biệt là tăng độ chính xác.
Theo tìm hiểu của PV, quy trình xét nghiệm của CDC Hoa Kỳ đưa ra lúc ban đầu phát hiện 3 gene N1, N2 và N3 của SARS-CoV-2. Tuy nhiên, sau đó quy trình cập nhật ngày 30/3/2020 của CDC Hoa Kỳ đã loại bỏ gene N3 chỉ giữ lại gene N1 và N2. Việc loại gene N3 ở đây là để quy trình đơn giản và chính xác hơn. Việc thay đổi này cả thế giới đều biết và Bộ Y tế Việt Nam cũng đã cập nhật trong các hướng dẫn.

Hiện đa số nhà sản xuất tham khảo quy trình của WHO thì dùng gene E và RdRp, nhà sản xuất nào tham khảo quy trình của CDC Hoa Kỳ thì dùng gene N1 và N2 theo hướng dẫn cập nhật mới nhất, không còn nhà sản xuất dùng gene N3 trong kit.
Thế nhưng vừa qua, Bộ kit xét nghiệm Covid-19 có chứa thành phần phát hiện gene N3 đã trúng gói thầu tại Bệnh viện Nhi Trung ương.
Theo đó, ngày 9/12/2020, Bệnh viện Nhi Trung ương (thay mặt Bộ Y tế đứng ra tổ chức) có ra quyết định số 7760/QĐ-BVNTƯ về việc phê duyệt kết quả trúng thầu cho 1 công ty sản xuất trong nước về gói thầu mua sắm kit real-time RT-PCR phát hiện SARS-CoV-2. Cụ thể, theo tìm hiểu của PV, Hồ sơ mời thầu (HSMT) do Bệnh viện Nhi Trung ương phát hành có 7 yêu cầu kỹ thuật chính. Bao gồm:
1. Nguyên lý: Phát hiện virus SARS-CoV-2 bằng phương pháp Real-time OneStep RT-PCR trong mẫu đường hô hấp trên và đường hô hấp dưới.
2. Gen đích: Là gene N hoặc gene E hoặc cả gene E và gene N theo tài liệu mới nhất của CDC Mỹ, WHO và được phát hiện chỉ trong 1 phản ứng.
3. Thời gian phát hiện trên máy RT-PCR: ≤ 150 phút.
4. Độ đặc hiệu lâm sàng: 100%.
5. Tích hợp chứng nội trong bộ kit để loại bỏ âm tính giả do quá trình lấy mẫu, xử lý mẫu.
6. Giới hạn phát hiện (LOD): ≤ 5 copy/ µL.
7. Thích hợp tối thiểu với các hệ thống real time PCR sau: Agilent: Stratagene Mx3000P, Stratagene Mx3005P, AriaMX. Analytik Jena: qTOWER. Applied Biosystems: ABI StepOne, ABI StepOne Plus, ABI 7300/7500, ABI 7500 Fast. Bio-Rad: iQ5 Multicolor, iCycler, CFX96, CFX96 Touch. DNA-Technology: DTprime 4M1, DTprime 5M1, DTlite. Eppendorf: RealPlex4. IT-TS Life: MyGo Pro, MyGo Mini. Qiagen: Rotor-Gene Q5 Plex. Roche: LightCycler 96. Sacace Biotechnologies: SaCycler-96. Thermo Fisher Scientific: QuanStudio 3, QuanStudio 5.
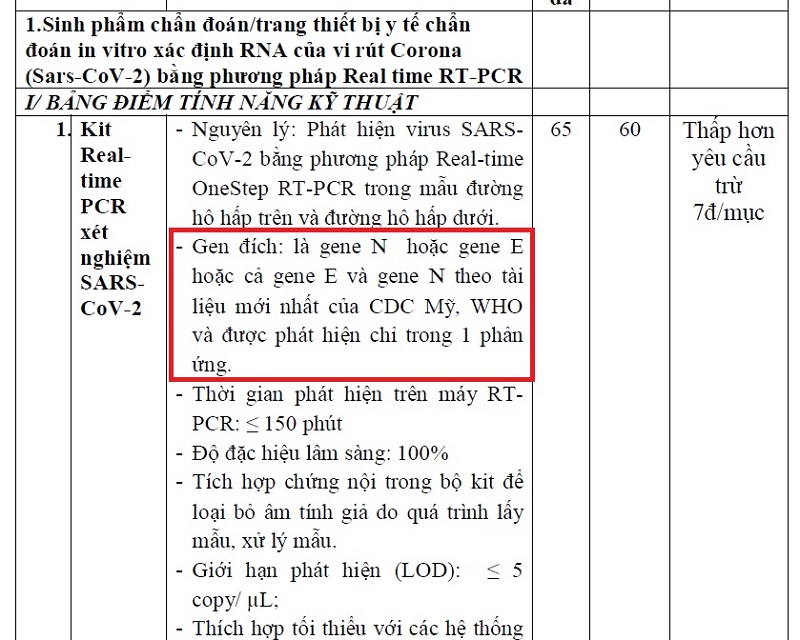
Với 7 yêu cầu này, số điểm tối đa là 65 điểm, số điểm tối thiểu là 60 điểm, nếu thấp hơn yêu cầu sẽ trừ 7 điểm/mục, số điểm yêu cầu kỹ thuật phải bằng hoặc vượt mức điểm tối thiểu mới được tiếp tục xem xét về tài chính.
Trong khi đó, theo quyết định số 5071/QĐ-BYT ngày 04/12/2020 về việc “Ban hành danh mục 02 trang thiết bị y tế được cấp số lưu hành tại Việt Nam” thì tại Việt Nam có 2 công ty sản xuất kit xét nghiệm SARS-CoV-2.
Theo tìm tìm hiểu của chúng tôi trong quyết định số 5071/QĐ-BYT cũng như quy trình kit xét nghiệm của 2 công ty này thì cả 2 đều dựa trên tài liệu của CDC Hoa Kỳ để phát triển bộ kit của mình, 1 công ty phát hiện 2 gene N1 và N2 theo cập nhật mới nhất của CDC Hoa Kỳ, còn 1 công ty thì phát hiện 3 gene N1, N2 và N3 theo hướng dẫn ban đầu của CDC Hoa Kỳ.
Trong quyết định số 7760/QĐ-BVNTƯ của Bệnh viện Nhi Trung ương thì công ty có kit phát hiện 3 gene N1, N2 và N3 đã trúng thầu. Nếu theo yêu cầu số 2 của HSMT thì tổng điểm của công ty có kit phát hiện 3 gene N1, N2 và N3 có đạt mức tối thiểu (60 điểm) để trúng thầu hay không?
Chúng tôi sẽ tiếp tục thông tin sự việc!
theo Tiến Đạt – Tiểu Thúy (theo tieudung)


